Was ist Entropie und wie steht diese im Zusammenhang mit Energie? – Teil 3 der Serie Energieeffizienz einfach erklärt
 Im letzten Teil dieser Serie haben wir gesehen, dass Energie aus zwei Bestandteilen besteht: dem zur Verrichtung einer Arbeit nutzbaren Anteil (Exergie) und einem nicht nutzbaren Anteil (Anergie). Je höher der Exergieanteil, desto höher ist die „Qualität“ der Energie; und die Nutzung eines Energieträgers mit einer dem Verwendungszweck angemessenen Qualität (einem angemessenen Exergieanteil) ist ein Beitrag zur Verbesserung des Energieeinsatzes und damit der energiebezogenen Leistung. Um den Exergieanteil zu quantifizieren und zu verstehen, warum die verschiedenen Energieformen nicht unbegrenzt ineinander umgewandelt werden können, müssen wir die Entropie verstehen. In diesem Teil wollen wir uns ansehen, was sich hinter der Entropie verbirgt und dieses Wissen auf energierelevante Prozesse anwenden, wo sie eine Rolle spielt – etwa der Stromerzeugung in einem Wärmekraftwerk. Hieraus lassen sich allgemeine Schlussfolgerungen für den Zusammenhang zwischen Entropie und Energieeffizienz ableiten, welche wir uns in diesem Beitrag ansehen möchten.
Im letzten Teil dieser Serie haben wir gesehen, dass Energie aus zwei Bestandteilen besteht: dem zur Verrichtung einer Arbeit nutzbaren Anteil (Exergie) und einem nicht nutzbaren Anteil (Anergie). Je höher der Exergieanteil, desto höher ist die „Qualität“ der Energie; und die Nutzung eines Energieträgers mit einer dem Verwendungszweck angemessenen Qualität (einem angemessenen Exergieanteil) ist ein Beitrag zur Verbesserung des Energieeinsatzes und damit der energiebezogenen Leistung. Um den Exergieanteil zu quantifizieren und zu verstehen, warum die verschiedenen Energieformen nicht unbegrenzt ineinander umgewandelt werden können, müssen wir die Entropie verstehen. In diesem Teil wollen wir uns ansehen, was sich hinter der Entropie verbirgt und dieses Wissen auf energierelevante Prozesse anwenden, wo sie eine Rolle spielt – etwa der Stromerzeugung in einem Wärmekraftwerk. Hieraus lassen sich allgemeine Schlussfolgerungen für den Zusammenhang zwischen Entropie und Energieeffizienz ableiten, welche wir uns in diesem Beitrag ansehen möchten.
Weitere Beiträge aus unserer Serie Energieeffizienz einfach erklärt:
Teil 1: Dies ist die Bedeutung der Energieeffizienz
Teil 2: Von der Energieeffizienz zur Energiequalität
Teil 3: Was ist Entropie und wie steht diese im Zusammenhang mit Energie?
Teil 4: Was ist Energie und welche Bedeutung hat sie?
Teil 5: Energieverbrauch in Deutschland – relevante Einsparpotenziale in Wirtschaft und Industrie
Teil 6: Die Prozesswärme in der Industrie als größter Energieverbraucher
Teil 7: Abwärmenutzung in der Industrie – Ermitteln Sie Ihre Potenziale mit der Pinch Analyse
Teil 8: Raumwärme und Warmwasser als Energieträger – So verbessern Sie Ihre Energieeffizienz
Teil 9: So verbessern Sie Ihre Energieeffizienz bei der Nutzung von Prozesskälte und Klimakälte
Teil 10: Energieeffiziente Elektromotoren und Pumpen als Querschnittstechnologien
Teil 11: So verbessern Sie Ihre Energieeffizienz durch energieeffiziente Beleuchtung am Arbeitsplatz
Teil 12: Energieeffizienz in der Informations- und Kommunikationstechnik
Teil 13: Energieeffizienz im Verkehr
Die Bedeutung der Entropie steht im engen Zusammenhang mit der Energie
Einen ersten Ansatz zur Quantifizierung von Exergie haben wir schon im Teil III dieser Serie kennengelernt: Der Exergieanteil von Wärme hängt von der Differenz zur Umgebungstemperatur ab – er ist umso höher, je größer diese Differenz ist. Da in Wärmekraftwerken nur der Exergieanteil der Wärme in Strom umgewandelt werden kann, sind auch diese umso effiziente, je höher die Temperatur ist, mit der sie arbeiten (und in der Praxis begrenzen die Materialstabilität und Sicherheitsanforderungen die mögliche Temperatur). Was wir nicht erörtert haben, sind die Gründe hierfür. Erklärt wird beides durch den 2. Hauptsatz der Thermodynamik, der – in vielen möglichen Formulierungen – besagt, dass in einem isolierten System die Entropie niemals abnimmt – sie darf also gleichbleiben oder zunehmen, aber nicht kleiner werden. Um das in Teil III beschriebene Verhalten von Energie wirklich verstehen zu können, müssen wir uns mit diesem 2. Hauptsatz beschäftigen. Zunächst besagt er, dass es eine Größe namens Entropie gibt und dass diese Größe bei Energieumwandlungen in einem isolierten System entweder gleichbleibt oder aber zunimmt, also erzeugt werden kann. Dabei heißt isoliertes System: ein System, dass mit seiner Umgebung weder Energie noch Materie austauscht.
Schulung Basiswissen Energieeffizienz
Lernen Sie in der Schulung Basiswissen Energieeffizienz die Bedeutung der Energieeffizienz kennen und erfahren Sie, wie Sie Ihren Energieeinsatz im Unternehmen optimieren.

Der Siegeszug der Dampfmaschine steht im engen Zusammenhang mit der Entropie
Die Entdeckung der Entropie geht zurück auf die Erfindung der Dampfmaschine. Die erste brauchbare Dampfmaschine hatte der englische Schmied Thomas Newcomen 1712 gebaut, um Grundwasser aus den immer tiefer liegenden Kohleschächten abpumpen zu können: Dampf wurde in einen Zylinder geleitet, durch eingespritztes kaltes Wasser zur Kondensation gebracht und damit ein Unterdruck erzeugt, der einen Kolben nach unten zog. Dieser Kolben war über ein Balancier mit einem Gegengewicht, der eigentlichen Pumpvorrichtung, verbunden, die bei diesem Vorgang nach oben gezogen wurde. Diese Dampfmaschine wurde nicht nur in den Kohlerevieren Englands, sondern auch Schwedens, Deutschlands und Frankreichs eingesetzt. Aber auch nur dort: sie verbrauchte so viel Kohle, dass sie nur wirtschaftlich war, wo es Kohle fast umsonst gab. Als der an der Universität Glasgow arbeitende schottische Instrumentenbauer James Watt eine solche Dampfmaschine reparieren sollte, begann er, sich mit den Ursachen für ihren schlechten Wirkungsgrad zu beschäftigen. Eine Ursache erkannte er darin, dass mit dem Dampf und dem eingespritzten Wasser auch der Zylinder immer wieder erhitzt und abgekühlt wurde, was viel Energie kostete. Er fand auch die Lösung und baute eine Dampfmaschine, in der der Dampf in einem separaten kalten Behälter, dem Kondensator, kondensierte. Zugleich nutzte er den Dampf, um den Zylinder warm zu halten und um das Absinken des Kolbens mit leichtem Überdruck zu unterstützen. Diese 1769 patentierten Verbesserungen der Dampfmaschine und weitere Erfindungen Watts, wie die Getriebe zur Umwandlung des Kolbenhubes in eine Drehbewegung oder die doppelwirkende Dampfmaschine, bei der der Dampf abwechselnd auf beide Seiten des Kolbens geleitet wurde und somit Auf und Abwärtsbewegung antrieb, verbesserten den Wirkungsgrad soweit, dass die Dampfmaschine auch jenseits der Kohlegruben zur universellen Antriebsmaschine der Industriellen Revolution wurde. Alleine in Cornwall waren im Jahr 1800 55 Wattsche Dampfmaschinen installiert.

Grenzen der Energieeffizienz
Watt erreichte seine Verbesserungen durch Beobachtungen und physikalische Überlegungen, war aber vor allem am praktischen Nutzen interessiert. Grundlegend theoretisch durchdrungen wurde die Dampfmaschine aber erst 1824 von dem französischen Physiker Sadi Carnot, der damit die Wärmelehre (Thermodynamik) begründete. Carnot konnte dabei auf die Gasgesetze zurückgreifen, namentlich auf das von Boyle-Mariotte (bei gleichbleibender Temperatur ist der Druck eines Gases umgekehrt proportional zu seinem Volumen) und Guy-Lussac (bei gleichbleibendem Druck ist das Volumen proportional der Temperatur). Den Ablauf in einer idealen Dampfmaschine zerlegte er gedanklich in vier Schritte:
- Wird das Dampfventil geöffnet und strömt Dampf in den Zylinder, wird Wärme vom heißen Temperaturreservoir (dem Dampfbehälter) aufgenommen.
- Wird das Dampfventil geschlossen, expandiert der Dampf und kühlt dabei ab; durch die Expansion wird mechanische Arbeit verrichtet.
- Durch das eingespritzte Wasser geht Wärme vom Dampf in das Wasser über, das Volumen des Dampfes verringert sich wieder.
- Durch den Luftdruck auf den Kolben wird das Gas verdichtet, dabei wird mechanische Arbeit verrichtet.
Carnot erkannte, dass die Bewegung, die mit der Dampfmaschine erzeugt wird, letztlich auf das Bestreben der Wärme, von einem heißen zu einem kalten Reservoir zu fließen, zurückgeht, und dass die geleistete Arbeit proportional zu dem Temperaturunterschied zwischen diesen beiden Reservoirs ist. Daraus ermittelt er einen theoretisch höchstmöglichen Wirkungsgrad:
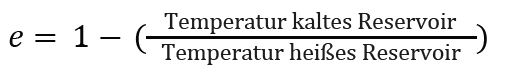
1834 stellt der französische Physiker Benoît Clapeyron den Ablauf des Carnot-Zyklus grafisch dar. Vorgänge, die bei gleichbleibender Temperatur ablaufen, werden „isotherm“ genannt. Solche, bei denen keine Wärme mit der Umgebung ausgetauscht werden, werden „adiabatisch“ genannt. Daher kann man die vier Schritte auch so bezeichnen:
- isotherme Expansion,
- adiabatische Expansion,
- isotherme Kompression,
- adiabatische Kompression.
Video: Revision ISO 50001:2018
Video: ISO 50001 – Überblick über die Norm
Die Entdeckung der Wärme als Energieform
Carnot dachte noch, wie zu seiner Zeit die meisten Forscher, dass Wärme eine („Caloricum“ genannte) Substanz sei und daher nicht verloren gehen könne. Der englische Erfinder Graf Rumford hatte allerdings Ende des 18. Jahrhundert bereits bemerkt, dass sich Kanonenrohre, die aufgebohrt wurden, erwärmen, und vermutete daher, dass Wärme eine Form von Bewegung sei. Mitte des 19. Jahrhunderts entdeckten Mayer, Joule und Helmholtz, dass Wärme eine Energieform ist; Helmholtz formulierte den 1. Hauptsatz der Thermodynamik (nach dem Energie eine Erhaltungsgröße ist: in einem isolierten System bleibt die Energie gleich – oder: Energie kann weder erzeugt werden noch verloren gehen).
Starten Sie jetzt den kostenlosen E-Learning Kurs Umweltmanagement DIN EN ISO 14001!
Dieser E-Learning Kurs bietet Ihnen einen schnellen und einfachen Einstieg ins Umweltmanagement nach ISO 14001. Wir machen Sie dabei mit der Umweltmanagement Definition vertraut und zeigen, was man unter einem Umweltmanagementsystem nach ISO 14001 oder EMAS versteht.
Auch Mayer, Joule und Helmholtz leisteten einen Beitrag zur Entdeckung der Entropie
Dem deutschen Mediziner Julius Robert Mayer fiel als Schiffsarzt auf dem holländischen Dreimaster Java auf, dass das venöse Blut seiner Patienten in den Tropen heller war als im heimischen Deutschland. Er schloss, dass es weniger oxidiert sei, da der Körper bei tropischen Temperaturen weniger Wärme produzieren muss. Nach seiner Rückkehr beschäftigte ihn die Frage, ob nicht auch die Wärme, die bei Muskelarbeit entsteht, auf die Oxidation von Blut zurückgeht und vermutete, dass Bewegungsenergie in Wärme umgewandelt werden könne – Wärme also eine Form von Energie war. Dieser Vermutung nachgehend zeigte er, dass Wasser durch Schütteln erwärmt werden konnte und veröffentlichte 1842 einen ersten Wert zur Umrechnung von Bewegungs- in Wärmeenergie. Unabhängig von Mayer führte der britische Physiker James Prescott Joule zur gleichen Zeit thermodynamische Untersuchungen durch. Joule war hierzu durch die Entdeckung angeregt worden, dass sich elektrische Leiter bei Stromdurchfluss erwärmten; und auch er entdeckte, dass Wasser durch mechanische Bewegung erwärmt werden konnte. Seine Entdeckungen und genaue Messungen hierzu veröffentlichte er 1850 und verwendete erstmals die Begriffe elektrisches und mechanisches Wärmeäquivalent. Der deutsche Physiker Hermann von Helmholtz verfasste 1846 eine Arbeit „Über den Stoffwechselverbrauch bei Muskelaktionen” und veröffentlichte 1847 das Buch „Über die Erhaltung der Kraft”, in dem er den Energieerhaltungssatz herleitete und begründete.
Video: ISO 50001 – Abschnitt 4.1 Kontext der Organisation
Video: ISO 50001 – Abschnitt 5.2 Energiepolitik
Die Entdeckung der Entropie in der Energie
1848 zeigte dann der britische Physikprofessor William Thomson (der spätere Lord Kelvin), dass zwischen Carnots Annahmen und dem ersten Hauptsatz der Thermodynamik ein Widerspruch besteht: Im Carnot-Prozess blieb die Wärme erhalten, aber gleichzeitig wurde eine Arbeit verrichtet – es wurde also Energie erzeugt. Diesen Widerspruch löste 1850 der deutsche Physiker Rudolf Clausius auf, der den Carnot-Prozess genauer untersuchte und feststellte, dass bei jedem Schritt die aufgenommene Wärme und die verrichtete Arbeit – mit dem Wärmeäquivalent berechnet – einen konstanten Wert ergaben, den Thomson später „innere Energie“ U nannte:
dU = dQ + dW
(d steht für Differenz – die innere Energie eines Systems ändert sich also mit zu oder abgeführter Wärme und zugeführter oder geleisteter Arbeit).
Clausius zeigte, dass im Carnot-Prozess nicht, wie von Carnot angenommen, die zu- und die abgeführte Wärme gleich waren, sondern nur der Teil der Wärme, der nicht in mechanische Arbeit umgewandelt wurde, auf das kalte Wasser übertragen wird. Damit erwies sich der Energieerhaltungssatz als richtig. Dieser konnte aber nicht erklären, warum Wärme immer von einem warmen zu einem kalten Körper fließt (was schon Carnot als treibende Kraft erkannt hatte) und niemals in umgekehrter Richtung. Clausius erkannte aber, dass im Carnot-Prozess nicht nur die geleistete Arbeit proportional der Temperaturdifferenz zwischen dem warmen und alten Reservoir ist, sondern dass das Verhältnis von übertragener Wärme zu absoluter Temperatur in beiden Reservoirs gleich war:
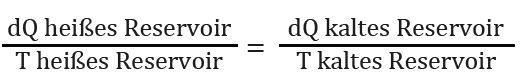
Wenn dieses Verhältnis aber konstant ist, kann es auch als eigene Größe beschrieben werden:
dS = dQ/T.
In der Natur laufen nur Vorgänge ab, bei denen dS positiv ist. 1865 prägte Clausius für S den Begriff Entropie (ein Kunstwort aus dem griechischen entrepein = umwandeln und tropé = Wandlungspotenzial).
Und was ist Entropie nun? Hier finden Sie eine Erklärung
Was ist eigentlich die Entropie? Mit der Entropie hatte Clausius eine Größe gefunden, die wie Druck oder Temperatur eine Zustandsgröße war, mit der ein System beschrieben werden kann und die zeigte, in welche Richtung in der Natur Prozesse spontan ablaufen können. Damit hatte er den zweiten Hauptsatz der Thermodynamik entdeckt. Dass Wärme spontan immer nur von einem warmen zu einem kalten Körper fließt, zeigt, dass hierbei die Entropie zunimmt (Andere Energieflüsse – wie etwa die Klimatisierung von Räumen – sind nur möglich, wenn in einem verbundenen System Energie umgewandelt und dabei Entropie mit übertragen wird.). Clausius hatte zwar den zweiten Hauptsatz der Thermodynamik mathematisch formuliert, konnte aber nicht erklären, was Entropie eigentlich war. Dies gelang erst dem österreichischen Physiker Ludwig Boltzmann, einem der Begründer der kinetischen Gastheorie. Diese erklärt die makroskopischen – also die mit Hilfe von Experimenten und Messungen ermittelbaren – Eigenschaften von Gasen aus der Summe ihrer mikroskopischen Eigenschaften, also der Eigenschaften der winzigen Teilchen, aus denen ein Gas besteht. So wird etwa die Temperatur eines Gases durch die Wärme erklärt, die durch Zusammenstöße der Gasteilchen untereinander und mit der Behälterwand übertragen wird. Die kinetische Gastheorie verbindet so die Gesetze der klassischen Mechanik (die die Bewegungsenergie der einzelnen Gasteilchen beschreiben) mit denen der Thermodynamik: eine höhere Geschwindigkeit der Gasteilchen (höhere kinetische Energie) messen wir makroskopisch als höhere Temperatur. Diese „thermische Bewegung“ der Gasteilchen ist auch der wesentliche (bei Edelgasen sogar der einzige) Bestandteil von Clausius‘ innerer Energie U (bei Nicht-Edelgasen kommen andere Beiträge, wie die Rotations- und Schwingungsenergie von Molekülen oder die Bindungsenergie zwischen den Molekülen hinzu); die Gesamtenergie eines Systems setzt sich aus mikroskopischen Energieformen – wie der inneren Energie U – und den makroskopischen Energieformen – wie der kinetischen Energie – zusammen.
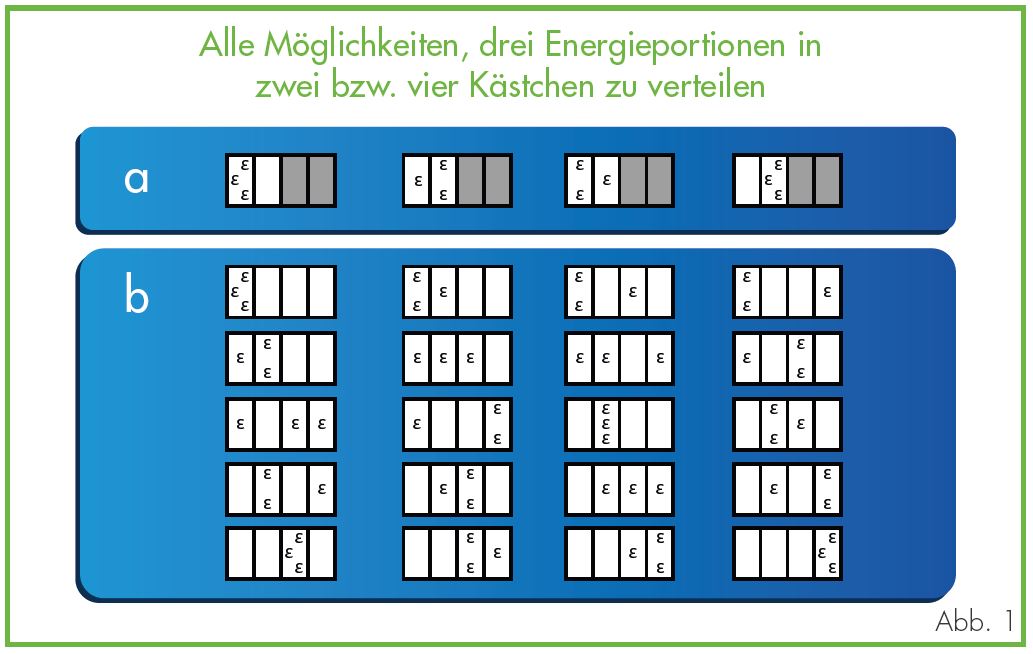
Boltzmann erkannte 1877 aber noch einen weiteren Zusammenhang:
Aus den Mikrozuständen eines Gases konnte man auf makroskopische Zustände wie die Temperatur schließen, umgekehrt war dies aber nicht möglich – die Temperatur eines Gases war mit einer sehr großen Zahl von Mikrozuständen wie Ort und Geschwindigkeit der Gasteilchen vereinbar. Die Entropie, so erkannte er, war ein Maß für die Anzahl der möglichen Mikrozustände eines Systems, die einen Makrozustand ergeben. Boltzmann dachte sich Energie hierzu als in kleine „Energieportionen“ aufgeteilt und die möglichen mikroskopischen Zustände als „Kästen“, in denen diese Portionen abgelegt werden. So gibt es vier Möglichkeiten, drei „Energieportionen“ auf zwei Kästen zu verteilen. Verdoppeln wir das Volumen des Behälters, stellen also vier Kästen bereit, gibt es bereits 20 Möglichkeiten, die „Energieportionen“ zu verteilen. Dieses Gedankenexperiment entspricht etwa einem Gasbehälter, der zunächst durch eine Trennwand in zwei Hälften geteilt ist; nur in einer Hälfte befindet sich Gas. Wird die Trennwand entfernt, steht dem Gas doppelt so viel Raum („Kästen“) zur Verfügung. Da alle Verteilungsmöglichkeitenstatistisch gleich wahrscheinlich sind, beträgt die Wahrscheinlichkeit, dass sich alle drei „Energieportionen“ in einem Kasten wiederfinden, im ersten Beispiel 50 %, im zweiten nur noch 4/20 = 5 %. Das Gas wird sich also mit größerer Wahrscheinlichkeit auf mehrere „Kästen“ verteilen und ganz analog, stellte sich Boltzmann vor, würde sich Energie auf die möglichen Mikrozustände verteilen. Die Entropie ist ein Maß für Zerstreuung der Energie (gemessen wird genauer der Logarithmus der Anzahl möglicher Mikrozustände (W) – die Entropie zweier Systeme besteht aus der Summe ihrer einzelnen Entropien, die Zahl der Mikrozustände der beiden Systeme ist aber multiplikativ, daher muss sie logarithmiert werden:
S = k · log W, k ist eine Konstante).
Sie ist zugleich ein Maß für die „Qualität“ der Energie, denn diese geht mit zunehmender Zerstreuung zurück. Wenn Energie sich bei Umwandlungsprozessen zerstreut, wird Entropie erzeugt. Mit dieser Erkenntnis wird auch nachvollziehbar, warum Vorgänge spontan nur in Richtung wachsender Entropie ablaufen: die Zerstreuung von Energie ist – analog zur Ausbreitung von Gas in einem Behälter – einfach viel wahrscheinlicher als ihr Gegenteil (und da „Energieportionen“ sehr klein sind und ihre Anzahl schon bei kleinsten Energien extrem groß – so extrem wahrscheinlich, dass das Gegenteil noch nie beobachtet wurde). Ein Körper mit höherer Temperatur hat eine höhere Entropie als ein Körper mit niedrigerer Temperatur (da die Teilchen im wärmeren Körper sich intensiver bewegen), daher fließt Wärme nicht von einem kalten zu einem warmen Körper. Boltzmanns Gedankenexperiment war viel näher an der Realität, als er wissen konnte: Nach der Quantenmechanik ist Energie tatsächlich „gequantelt“, besteht also aus winzigen „Energieportionen“; und 1907 zeigte Albert Einstein, dass sich mit der Verteilung von „Energieportionen“ auf die Schwingungszustände von Atomen in einem Festkörper die Wärmekapazität von Festkörpern herleiten lässt. Diese sollte von der Temperatur abhängen, was mit den Messwerten bestens übereinstimmte und eine glänzende Bestätigung für Boltzmanns Theorie war.
Kostenlose Stellenbeschreibung Energiemanagement Beauftragter ISO 50001
Mit der kostenlosen Stellenbeschreibung Energiemanagement Beauftragter ISO 50001 definieren Sie dessen Aufgaben und Verantwortlichkeiten für Ihr Unternehmen.

Anwendung der Entropie im Zusammenhang mit der Energie
Entropie ist also eine Zustandsgröße von (thermodynamischen) Systemen. Was passiert aber bei Prozessen – schließlich wird Energie ja genutzt, um eine Arbeit zu verrichten? Entropie ist – anders als Energie – keine Erhaltungsgröße, sondern kann innerhalb eines Systems erzeugt werden. Sie kann aber auch – wie Energie – übertragen werden, also über die Systemgrenze zu- oder abgeführt werden. Eine Entropieänderung kann auf beide Vorgänge zurückgehen: dS = deS + diS (s. auch Abb. 2). (d steht für Differenz, deS steht für extern, also zu- oder abgeführte Entropie, diS für innerhalb des Systems erzeugte Entropie) Wird bei einem Prozess ausschließlich Wärme übertragen, spielt nur die zugeführte Entropie deS eine Rolle: aufgrund der Formel dS = dQ/T (siehe voriger Teil dieser Serie), wird einem System Entropie zugeführt, wenn es erwärmt wird; durch Wärmeabfuhr (Kühlung) kann die Entropie eines Systems verringert werden. Bei der Wärmeübertragung innerhalb der Systemgrenzen ist zu beachten, dass die mit der Wärme übertragene Entropie temperaturabhängig ist, wie die Umstellung der vorgenannten Formel zeigt:
dS = dQ/T T = dQ/dS
Je höher die Temperatur ist, desto weniger Entropie führt Wärme mit sich; Wärme niedriger Temperatur führt mehr Entropie mit sich. Wenn wir beispielsweise 10 Liter Wasser von 60 °C mit 10 Liter Wasser von 20 °C mischen, erhalten wir 20 Liter Wasser von 40 °C und eine Zunahme der Entropie. Rechnerisch werden nämlich 10 Liter Wasser von 60 °C auf 40 °C abgekühlt, und 10 Liter Wasser von 20 °C auf 40 °C erwärmt; und da die Entropieänderung bei der Abkühlung von 60 °C auf 40 °C geringer ist als die Entropiezunahme bei der Erwärmung der gleichen Menge, ergibt sich in der Summe eine Entropiezunahme.
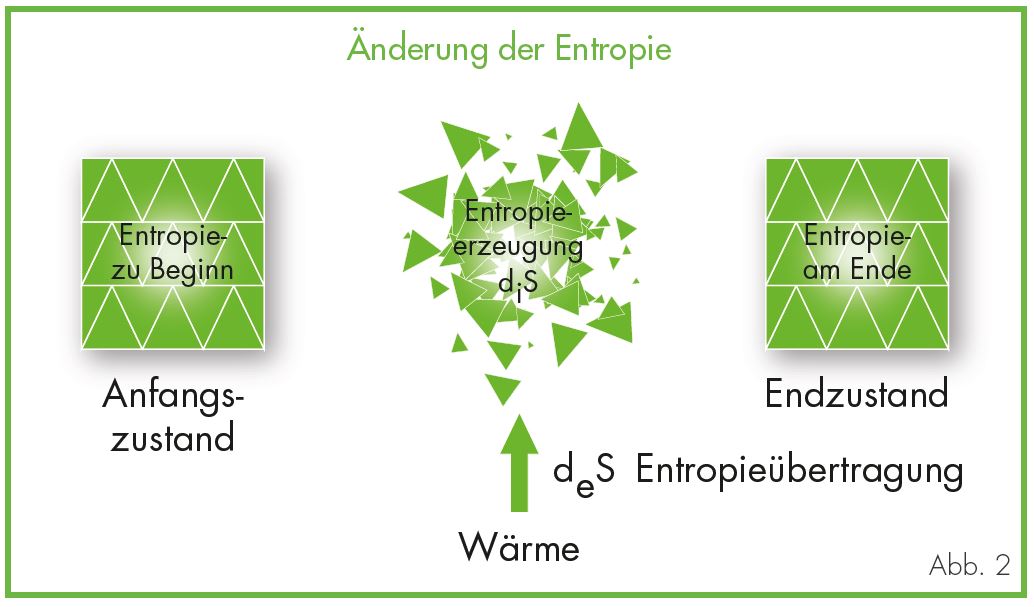
Dieses gilt allgemein:
Bei der Wärmeübertragung wird immer Entropie erzeugt – und zwar so lange, bis die Temperaturen beider Teilsysteme sich angeglichen haben und die Wärmeübertragung aufhört: dann hat das System seine maximale Entropie erreicht (d.h., die Energie hat sich soweit möglich zerstreut). Mit diesem Hintergrundwissen verstehen wir jetzt auch die grundlegenden energetischen Bedingungen in einem Wärmekraftwerk: Hier handelt es sich um einen Fließprozess. Solange die Verbrennung läuft, wird Wärme nachgeliefert, die aber aufgrund der enthaltenen Entropie nicht vollständig in Arbeit umgewandelt werden kann. Da Wärme bei hohen Temperaturen nur einen kleinen Anteil Entropie mit sich führt (siehe oben), ist der Wirkungsgrad (verrichtete Arbeit für eingesetzte Energie) desto besser, je höher die Arbeitstemperatur ist. Die zugeführte Entropie muss aber wieder abgeführt werden, und da der erzeugte Strom entropiefrei ist, muss die Entropie mittels Wärme abgeführt werden: das Kraftwerk muss gekühlt werden. Die Menge der abzuführenden Entropie bestimmt den Kühlbedarf – oder mit anderen Worten, den nicht zur Verrichtung von Arbeit nutzbaren Wärmeanteil, die Anergie. Diese lässt sich wieder aus der Formel dS = dQ/T berechnen: da die zugeführte Entropie Szu gleich der abgeführten Entropie Sab sein soll, ist
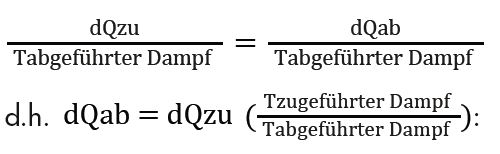
Je höher die Temperaturdifferenz, desto besser ist nicht nur der Wirkungsgrad, sondern desto geringer ist auch die Abwärmemenge. (Durch weitere Umstellung der Formel kann man auch den Wirkungsgrad berechnen: der zu Ehren von Sadi Carnot benannte Carnot-Faktor zeigt, welcher Anteil eines Wärmestroms maximal in Arbeit umgewandelt werden kann:
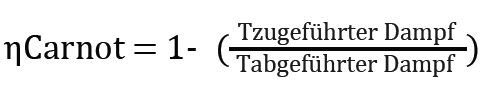
Dazu kommen Energieverluste bei der Dampferzeugung: Flammtemperaturen in Wärmekraftwerken liegen bei 1.200°C, der Dampf wird auf etwa 550°C erhitzt – auch hier wird Entropie erzeugt.
Entropie und Energieeffizienz einfach erklärt
Das Konzept der Entropie erklärt, warum bei der Stromerzeugung (und allen anderen Prozessen zur Umwandlung von Wärme in Arbeit, also z.B. auch in einem Verbrennungsmotor) Wärmeverluste auftreten müssen – die energetische Effizienz also prinzipiell begrenzt ist. Bei anderen Umwandlungen, etwa von elektrischen Strom in mechanische Arbeit, wird keine Entropie übertragen – sie entsteht nur, wenn durch Reibung Wärme erzeugt wird. So sind hohe (energetische) Wirkungsgrade möglich. Auch die direkte Umwandlung mechanischer Energie in Strom (Generator) ist energetisch hocheffizient; entscheidend ist, wie die antreibende mechanische Arbeit erzeugt wird: die direkte Nutzung von Bewegungsenergie, wie beispielsweise in Wasserkraftwerken oder Windrädern, ist hocheffizient. Ist die Umwandlung von Wärme in Arbeit unvermeidlich, kann der energetische Wirkungsgrad durch Nutzung der Abwärme vermindert werden: für viele Energieverbraucher reicht deren Energiequalität nämlich noch aus.
Ich wünsche Ihnen viel Erfolg.
Ihr Jürgen Paeger
 Gerne teilen wir unser Wissen mit Ihnen, bitte beachten Sie dennoch, dass die Inhalte der Blogbeiträge urheberrechtlich geschützt sind.
Gerne teilen wir unser Wissen mit Ihnen, bitte beachten Sie dennoch, dass die Inhalte der Blogbeiträge urheberrechtlich geschützt sind.
Durch die Publizierung der Blogbeiträge sind Sie daher nicht berechtigt, diese zu verkaufen, zu lizenzieren, zu vermieten oder anderweitig für einen Gegenwert zu übertragen oder zu nutzen. Sie sind weiterhin nicht berechtigt, die Inhalte der Blogbeiträge in eigenständigen Produkten, welche nur die Inhalte der Blogbeiträge selbst beinhalten oder als Teil eines anderen Produkts zu vertreiben. Weiterhin dürfen Inhalte dieses Blogs auch auszugsweise nur mit schriftlicher Genehmigung des Herausgebers verwendet werden.
Besten Dank für Ihr Verständnis.





3 Comments
Hallo Herr Paeger,
ich habe selten eine so schöne und verständliche Erklärung von Entropie gesehen. Vielen Dank für Ihren Beitrag.
Viele Grüße
Tobias Prager
Ich hätte nicht gedacht, dass die erste Dampfmaschine bereits 1712 gebaut wurde, die dafür sorgte, dass Grundwasser abgepumpt werden konnte. Ich bin aktuell auf der Suche nach einem Dampfkessel für meine Firma. Hoffentlich habe ich bis zum Ende der Woche einen passenden Fachbetrieb für industrielle Dampfkessel gefunden.
Wirklich eine sehr gute und auch eher verständliche Erklärung der Entropie!